

近年来,基于细胞替代疗法展现其在糖尿病(diabetesmellitus,DM)治疗上优越性。干细胞MSCs)因具多向分化潜能、低免疫原性、免疫调节作用、抗炎作用和抗凋亡作用等特性,被认为是目前干预糖尿病理想种子细胞。

糖尿病传统干预方法治标不治本
糖尿病(DM)属于慢性、非传染性疾病,以高血糖为主要表现,可累及身体各脏器如心脏、肾脏、眼底、大血管与组织产生副反应,最终导致功能减退或衰竭。
糖尿病分为三种:1型糖尿病(type1diabetesmellitus,T1DM)、2型糖尿病(type2diabetesmel-litus,T2DM)和妊娠期糖尿病。
三种糖尿病中前两种最常见,1型糖尿病是因体内免疫复合物攻击导致胰岛β细胞被破坏、胰岛素分泌不足所致;2型糖尿病约占所有糖尿病90%,其是因各种原因(包括遗传、环境等因素)导致胰岛素抵抗与胰岛素分泌不足(或相对不足)所致。

随着人们生活及饮食结构转变,糖尿病发病率日趋上升。中国糖尿病患者人数已超过1亿,50.4%成人处在糖尿病前期。糖尿病及副反应影响人类健康和生活质量。
面对目前严峻形势,该疾病尚无根治措施。常用人工合成胰岛素只能起到暂时缓解病情作用。因此,由于干细胞疗法诸多特征为干预糖尿病提供了方向。

干细胞疗法干预糖尿病分子机制介绍
目前干细胞疗法干预糖尿病分子机制尚未完全成熟,主要包括以下四种。
1.分化为产胰岛素细胞(insulin—producingcells,IPSC):干细胞分化为具有胰腺内分泌功能细胞是由关键转录因子调控(如Pdx-1、Ngn-3、NeuroD1、Pax4以及Pax6等)诱导干细胞分化为IPCS需正确重组这些细胞因子来激活分化旁路。
2.促进胰岛β细胞再生:除能直接分化为IPCS,干细胞还能通过迁移到受损胰岛细胞处促进内源性胰岛β细胞再生。
3.保护内源性胰岛β细胞:除再生能力外还具有免疫调节能力。干细胞疗法胞内低表达MHC—II蛋白与协同刺激分子,是一种免疫豁免细胞。
干细胞免疫抑制效应可减缓胰岛β细胞损毁自身免疫反应,同时还可提高胰岛细胞抗缺氧与氧化应激能力。
4.改善胰岛素抵抗:通过激活胰岛素受体底物—1(Insulinreceptorsubstrate—1,IRS—1)信号通路来改善高血糖,让葡萄糖转运蛋白-4(Glucosetransporter—4,GLUT—4)转位与表达增加,进一步使得周围胰岛素靶组织中胰岛素抵抗缓解。
干细胞疗法干预糖尿病临床研究证实效果良好
1.目前在“http://clinicaltrials.gov”网站注册有关干细胞干预糖尿病临床试验达145项,其中干细胞治疗2型糖尿病临床试验6个,以论文形式发表研究成果有13篇。
研究结果均显示干细胞可通过改善胰岛素β细胞功能或(和)改善外周靶组织胰岛素抵抗,能够有效改善糖尿病患者高血糖状态。
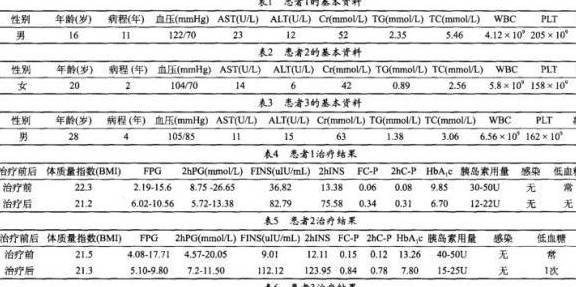
2.2013年9月昆明某医院内分泌科开展3例糖尿病临床研究,其患者年龄分别为16岁、20岁及28岁,体质质量指数分别为22.3、21.5及21.6。
所有患者运用干细胞疗法干预2次,间隔时间为一周一次。通过观察病情,术后无感染、出血及血栓副反应。患者均自述无明显不适,生命体征平稳,心肺腹无异常,双下肢无水肿,血糖平稳出院。
随访跟进,术后3个月血糖较前下降,控制平稳,低血糖明显减少,胰岛素剂量较前减少50%,空腹及餐后C肽较干预前升高8倍左右,未出现酮症等急性副反应。具体数据见下表:
综上所述,干细胞疗法干预糖尿病临床研究开展为糖尿病患者带来新希望,也为研究者及医生提供了新的突破口。希望各级部门加快推进干细胞临床研究进展,造福众多糖尿病患者。对此,你有什么看法?欢迎转发与留言!


 400-886-0919
400-886-0919











